비코로나 제품 매출 성장···'신드로믹 분자진단' 글로벌 공략
코로나19 수혜을 받았던 분자진단 전문기업 씨젠의 지난해 매출액이 1조원 아래로 떨어졌다.
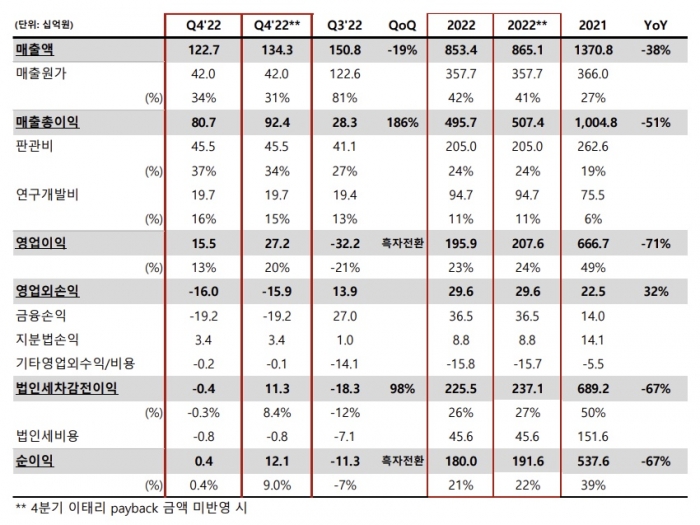
씨젠은 지난해 한국채택국제회계기준(K-IFRS)을 적용한 잠정 연간 매출액 8534억원, 영업이익 1959억원으로 잠정 집계됐다고 17일 공시했다.
이는 전년 대비 각각 37.7%, 70.6% 감소한 수치다.
이는 코로나19 진단시약 수요 감소 영향에 따른 것이다.
씨젠은 코로나19 유행 전인 2019년 매출액이 1220억원, 영업이익 224억원에 불과했으나 2020년부터 매출 1조1252억원, 영업이익 6762억원으로 각각 822%, 2915% 성장하고, 이듬해에도 매출 1조13708억원, 영업이익 6667억원으로 성장세를 이어갔다.
그러나 지난해부터는 많은 국가들이 코로나19 방역 규제를 더욱 완화하면서 코로나 진단시약의 매출이 감소했고, 이에 1분기에는 매출액 4515억원, 영업이익 1997억원, 2분기는 각각 1284억원, 130억원, 3분기는 1508억원, 영업손실 -322원으로 적자전환하며 하락세를 걸었다.
4분기도 매출액이 1227억원으로 전분기 대비 감소했으나 영업이익은 155억원을 기록해 흑자전환했다.
씨젠은 코로나 진단시약의 매출이 감소했으나 비코로나(Non-Covid) 제품 매출이 이를 상쇄하고 있고, 지속 성장 중이라는 입장이다.
실제로 호흡기질환(RV), 소화기감염증(GI), 인유두종바이러스(HPV), 성매개감염증(STI) 등 비코로나 진단시약의 4분기 매출은 522억원으로 전분기 대비 23%, 전년 동기 대비 40% 증가했다.
특히 4분기 시약 매출 중 비코로나 제품 비중이 53%, 코로나 제품 47%로 코로나19 발생 후 처음으로 비코로나 매출이 코로나 매출을 넘어섰다. 장비 부문에서는 4분기말 누적 기준으로 증폭장비 5429대, 추출장비 2828대가 설치되며 분자진단을 위한 인프라를 지속적으로 확대해 나갔다.
또 4분기에는 지난해 9월 처음으로 시행령이 발효된 이탈리아의 자금회수법(payback law) 관련 총 117억 비용이 발생해 매출과 영업이익 등에 영향을 미쳤다. 자금회수법은 이탈리아 정부에서 2015년 이후 의료 예산을 초과한 지출에 대해 기업으로부터 일부 회수하는 법이다. 해당 금액을 제외하면 4분기 영업이익은 272억원, 영업이익률은 20% 수준이다.
씨젠은 올해 다수의 특허 기술이 적용된 60여 종의 신드로믹(유사한 증상을 일으키는 병원체를 한꺼번에 검사해 원인을 찾는 검사법) 분자진단 제품과 완전 자동화 분자진단 시스템 AIOSTM를 기반으로 글로벌 분자진단 시장 공략을 지속한다는 계획이다.
최근 독일, 룩셈부르크, 벨기에 등 유럽 국가에서 동시검사의 보험수가가 신설 또는 확대되는 추세에 있는 만큼, 신드로믹 제품이 감염성 질병 검사와 환자관리에 가장 적합하다는 평가를 받는 것으로 씨젠 측은 보고 있다.
씨젠은 "신드로믹 분자진단 파이프라인과 이를 적용한 완전 자동화 분자진단 시스템을 기반으로 시장 변화에 신속히 대응하며 글로벌 표준화를 추진해 나갈 계획"이라고 전했다.
이와 함께 미국 현지에서는 제품 개발부터 임상, 인허가, 생산 및 판매까지 가능하도록 인프라 구축에 박차를 가하고 있다.
회사는 올 1분기 미국에서 연구용(RUO) 제품 현지 생산을 시작할 예정이다. 또 연내 미국 식품의약국(FDA)에 호흡기 제품에 대한 허가 신청 건을 접수하고, 내년부터 연 3개 이상의 신규 제품을 개발해 FDA 인증을 받도록 추진한다는 계획이다.

뉴스웨이 유수인 기자
suin@newsway.co.kr
저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지









댓글