iDMC 추가자료 요청, 3-2상 대상군 확대 또는 임상 중단 결정 재무 부담 없이 임상 진행 가능···기술이전 계획도'VM202' 가치 6.8~16조원 예상
김선영 헬릭스미스 대표는 28일 서울 마곡 본사에서 열린 기자간담회에서 "오늘 엔젠시스 3-2(두번째 3상)상 중간결과를 발표하고 싶었으나 지난 주말 iDMC가 추가 자료를 요정했다"며 "추가로 요청받은 자료는 안전성과 유효성 데이터 등으로 분석해가는 과정에서 여러 자료를 확인하는 것이다. 이에 따라 임상 진행과 관련한 결과는 7월 중 발표될 것으로 본다"고 밝혔다.
엔젠시스는 당뇨병성 신경병증, 당뇨병성 족부궤양 등 혈관이 막히거나 신경이 손상돼 나타나는 질환들을 타깃으로 하는 근육주사제다. 회사는 지난 2020년 6월 엔젠시스의 DPN에 대한 미국 3-2임상을 개시해 현재 기준 환자 152명 중 134명 등록을 완료했다.
헬릭스미스가 진행하는 3-2상은 항경련제 '가바펜틴'과 '프리가발린'을 복용하지 않는 DPN 환자를 대상으로 엔젠시스를 2회(각각16㎎) 투여하는 방식이다. 1차 평가변수는 180일째 7일 간 평균 통증 수치 변화이고 2차 평가변수는 180일째 7일 간 최악의 통증 수치 변화 및 통증이 50% 이상 감소한 반응자 비율이다. 90일째와 180일째 취침 전 감각 검사값, 180일째 반응자 비율, 90일째 7일 간의 일간 평균 통증 수치 변화 등을 분석한다. 추적기간은 6개월이고, 추가로 6개월을 연장해 안전성을 확인한다.
iDMC는 엔젠시스의 임상을 계속해도 되는지(지속), 대상 환자를 152명 이상인 153~250명 사이로 늘릴 것인지(수정), 아니면 임상 중단을 권고할 것인지를 판단하고 있다.
박영주 임상부문장은 "152명 절반인 76명 환자에 대한 180일 결과가 모아지면 통계전문가(CRO)와 데이터관리센터(CRO)에서 중간분석에 필요한 데이터를 iDMC 통계전문가에게 전달한다"며 "여기서 우리가 검증하려고 하는 것을 몇 퍼센트 확률로 검증할 수 있는지 등을 확인하는 '통계 조건부 검정력'을 계산해 iDMC와 공유한다"고 설명했다.
이어 "iDMC가 이를 검토해 만장일치로 결과를 내면 헬릭스미스에게 통보된다"며 "'기저값 대비 180일 시점에서의 통증 평균량 산출'(conditional power) 값이 39.6%보다 낮을 경우 임상 중단을 권고하고, 39.6%이상 80% 미만일 경우 대상자 재선정, 80% 이상일 경우 임상을 계속 할 수 있도록 권고한다"고 부연했다.
그러면서도 "다만 이것은 어디까지나 레코멘데이션(권고)이다"라고 강조했다.
김 대표는 iDMC 권고에 따라 임상 대상자 수를 늘리더라도 재정적 부담은 크지 않다는 입장이다. 김 대표는 "임상시험은 처음에 세팅할 때 비용이 들지 이미 진행 중인 건에 대해서 100명정도 추가하는 것은 큰 부담이 아니"라며 "우리가 계획하고 있는 임상 3상을 모두 완료한다고 가정했을 때 올해 말 기준 남는 자금은 800억원 정도다. 재무적 부담은 크지 않고 충분히 감당할 정도"라고 했다.
그는 임상 중단 권고를 받았을 경우에 대해 "위약대비 효과가 없는 임상은 진행하지 않을 것"이라면서도 "임상을 바로 끝내진 않을 것이다. 이미 약을 받은 환자들도 있고 추적관찰기간도 있기 때문에 환자를 마지막까지 케어할 의무에 따라 관리할 예정"이라고 말했다.
그러나 김 대표는 "의뢰자에게는 이중맹검(double blindness)이 유지되기 때문에, 임상 종료 시까지는 명확한 유효성 결과를 알 수는 없지만 여러 데이터를 감안할 때 좋은 결과를 얻을 것으로 기대하고 있다"고 전했다.
회사는 추가 3-3상도 진행한다는 방침이다. 임상 3-3상은 치료 횟수를 3회로 늘리고, 대상을 미국과 유럽으로 확장해 진행한다.
김 대표는 "미국 FDA에서는 두 개의 임상3상 결과를 요구한다. 임상 3-1상이 원래 성공했으면 임상을 한 번(3-2상)만 더하면 되는데 우리는 부분적으로 성공했기 때문에 3-3상을 하는 것"이라며 "3-3상은 조만간 시작해서 2024년 이전에 끝날 것으로 본다. 우리는 그 이전에 엔젠시스를 기술 이전하는 것이 목표"라고 말했다.
그는 "계획은 8월 초 3-2상 등록을 완료하고 내년 2~3월 정기주총 전 톱라인을 발표하는 것"이라며 "회사는 임상단계에 머무르지 않고 엔젠시스의 시판 허가 및 상용화 준비도 이미 시작했다. 현재 파트너사를 물색 중이며 기술이전, 공동개발, 투자유치 등을 논의하고 있다"고 전했다.
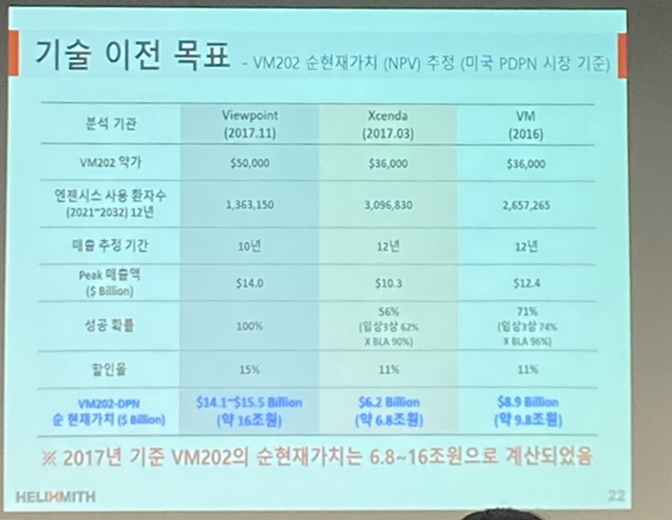
이어 김 대표는 기술수출 예상 규모에 대해 "순자산 가치를 계산하기 위해서는 약가, 환자수, 성공확률 등을 고려해야 한다"며 "현재 엔제시스의 가치는 2017년 기준 6.8조~16조원으로 계산됐다"고 덧붙였다.

뉴스웨이 유수인 기자
suin@newsway.co.kr
저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지










댓글